
En juin 2015, l’Office chinois des brevets (SIPO) a rejeté la demande de brevet au nom de Gilead, portant sur le Sofosbuvir un puissant inhibiteur d’une enzyme du virus de l’hépatite C.
L’Office a conclu que le Sofosbuvir correspond à une variante évidente d’un composé connu depuis 2005.
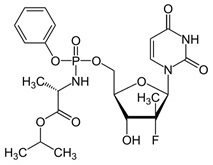
Le Sofosbuvir est un composé chimique inactif qui acquiert ses propriétés thérapeutiques in vivo lorsqu’il est partiellement dégradé par les cellules cibles. D’après le SIPO, une telle molécule peut être obtenue de manière évidente pour l’homme du métier.
Il faut rappeler que le Sofosbuvir (commercialisé sous la marque SovaldiTM) est, en association avec la ribavirine, le traitement le plus efficace pour le traitement de l’hépatite C chronique. En effet, sa spécificité pour la polymérase du virus (enzyme qui permet la multiplication de l’information génétique du virus) et son efficacité (près de 90% des patients atteints d’hépatite C) semblent avoir révolutionné le traitement d’une infection touchant près de 200 millions d’individus, dont près de 3,2% de la population chinoise.
Mais ce succès thérapeutique a un prix colossal : aux Etats-Unis, le prix du traitement est de l’ordre de 85 000 dollars pour 12 semaines de traitement. La raison vient probablement du rachat de la société Pharmasset (à l’origine de la conception de la molécule) pour une valeur de plus de 10 milliards de dollars.
La France et l’Allemagne ont abaissé le prix de commercialisation du traitement de 12 semaines à environ 40 000 euros après d’intenses négociations avec Gilead. Mais ce prix reste encore trop élevé pour les pays en voie de développement particulièrement touchés par le virus.
Un système de licence volontaire a été négocié avec 60 états où la prévalence du virus est importante pour la fabrication et la distribution à prix « plus accessible » (de 22 à 46% du prix américain). Cette licence couvre notamment l’Egypte et l’Inde, mais exclut la Chine.
Alors pourquoi ne pas recourir à une licence obligatoire prévue à l’article 31 de l’accord sur les droits de propriété intellectuelle qui touchent au commerce (accords ADPIC) ?
Les accords ADPIC autorisent en effet les « utilisations de l’objet d’un brevet sans l’autorisation du détenteur du droit, y compris l’utilisation par les pouvoirs publics ou des tiers autorisés par ceux-ci », en particulier pour des raisons de santé publique.
En 2008, la Chine a renforcé son dispositif légal concernant les licences obligatoires en matière de santé publique (“Measures for Compulsory Licensing of Patent Implementation Regarding Public Health” (Order No. 37)), qui ont encore été clarifiées en 2012 pour y inclure la notion de licence obligatoire pour « situation extraordinaire ou d’urgence » ou « intérêt public ».
Mais dans le cas du Sofosbuvir, la licence obligatoire aurait-elle été pertinente ?
Le rejet par le SIPO de la demande Gilead va éviter de répondre à cette épineuse question, car ce rejet va probablement permettre aux génériqueurs de proposer un équivalent à un prix bien plus attractif.
On notera que l’Egypte et l’Inde ont, malgré la licence volontaire, opté pour une invalidation des brevets, et qu’une opposition à l’encontre de brevet européen a été formée au motif que l’invention est dépourvue d’activité inventive, comme en Chine.
Mais Gilead dispose d’autres demandes de brevet en instance…
La saga du traitement de l’hépatite C est donc loin d’être terminée.
Article rédigé par Richard MONNI